Sinds in 1978 de eerste reageerbuisbaby werd geboren, is de gang naar de embryoloog bijna vanzelfsprekend geworden voor mensen die tevergeefs proberen op de natuurlijke manier zwanger te worden. Maar wat begon met basale bevruchting van een eicel in een petrischaaltje, is vandaag de dag uitgegroeid tot big business.
Niet elke ivf-behandeling resulteert direct in een zwangerschap. Statistisch gezien is dat ongeveer één op vier. “Eigenlijk niet eens weinig”, stelt klinisch embryoloog Sebastiaan Mastenbroek. “Als twee gezonde jonge mensen op het juiste moment in de cyclus seks hebben, is de kans op een zwangerschap gemiddeld óók maar zo’n twintig procent. Toch willen wij graag dat ivf-behandelingen succesvoller zijn dan dat, want ze zijn belastend voor de patiënt.”
Dat streven naar effectievere ivf leidde tot onderzoeken naar factoren die de kans op zwangerschap kunnen beïnvloeden. Daaruit kwamen allerlei technologieën die beogen die kans te vergroten. Amsterdam UMC is kritisch op zulke technologieën, zogenoemde ‘add-ons’. Eerst maar eens bewijzen dat ze veilig zijn en echt werken. Gynaecoloog en endocrinoloog Nils Lambalk: “Wij stellen als eis dat iets aantoonbaar effectief is voordat we het in de klinische praktijk toepassen.”
Assisted hatching
Er zijn ruim een dozijn van deze technieken, we noemen hier de bekendste. PGS (inmiddels omgedoopt in PGT-A) is sinds medio jaren 90 in zwang. De techniek wordt toegepast om uit de bevruchte embryo’s dat exemplaar te kiezen dat geen numerieke chromosomale afwijkingen lijkt te hebben.
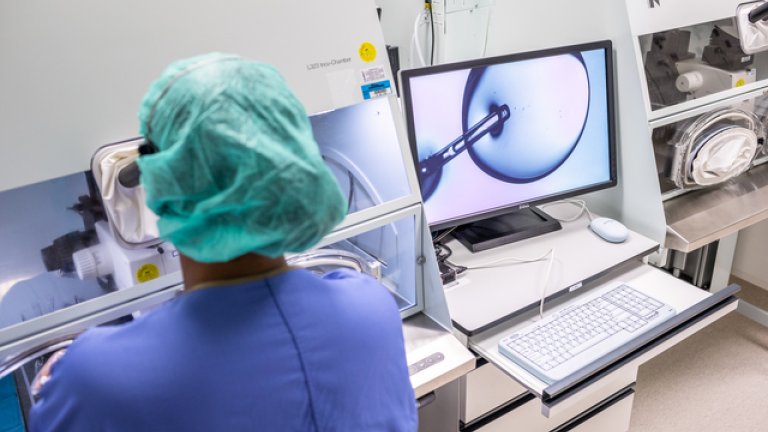
Time-lapse wil de keuze voor het beste embryo verbeteren door ze allemaal te filmen vanaf het moment van de bevruchting. Daarom is de incubator met de embryo’s voorzien van een camera.
Assisted hatching. Mastenbroek: “Wanneer het embryo in het laboratorium geselecteerd wordt voor plaatsing in de baarmoeder, zit daar nog een eiwitmantel omheen, de zona pellucida. Daarin kun je een gaatje maken, met de gedachte dat de kans op zwangerschap verhoogd zou kunnen worden, omdat het embryo dan als het ware makkelijker uit zijn ‘ei’ zou kunnen komen.”
Embryo-glue: er wordt een stofje toegevoegd aan de kweekvloeistof waarin het embryo ligt dat in de baarmoeder wordt geplaatst. Die ‘lijm’ zou innesteling moeten verbeteren.
Kerntransplantatie
Op de vraag of Amsterdam UMC werkt met deze add-ons in zijn voortplantingsgeneeskunde antwoordt Lambalk: “Nee. De conclusie van onderzoeken naar al deze technologieën is: ze leiden niet tot méér zwangerschappen. Terwijl dat in iedere folder van iedere ivf-kliniek ter wereld wel botweg staat. Dat is gewoon niet waar. Een aantal levert zelfs mínder zwangerschappen op.”
Dan is er nog kerntransplantatie. Niet zomaar een add-on, deze techniek is van een heel andere orde. Lambalk legt uit: “Mensen willen bij voorkeur een genetisch eigen kind. Maar als je veertig bent, zijn je bevruchte eicel en de kern erin ook veertig jaar oud. Om de kern in die eicel zit een soort soep: cytoplasma, met daarin bijvoorbeeld mitochondriën, de energiefabriekjes van de cel, en eiwitten. Die zijn nodig voor succesvolle celdeling. Dat de celdeling bij oudere eicellen vaak fout gaat, wordt onder meer veroorzaakt door processen in dat cytoplasma.
Gevoelig
“Als je het kernmateriaal van die oudere vrouw plaatst in de eicel van een jonge vrouw, met jong cytoplasma en jonge mitochondriën, levert dat een vitaler embryo op. Juist de kern is voor de wensmoeder van belang: daarin zitten de gegevens van je vader en moeder, je opa en oma.
“Maar. Kerntransplantatie is makkelijker gezegd dan gedaan. Het is een zware operatieve ingreep aan de eicel, waarvan we nog niet weten wat voor implicaties die op termijn heeft voor het kind.”
Het principe van kerntransplantatie ligt gevoelig, benadrukken Lambalk en Mastenbroek, omdat het kind dat eruit voortkomt genetisch gezien drie ouders heeft. Lambalk: “Ik heb hier in principe geen problemen mee; maar sommige religieuze stromingen wel.” Kerntransplantatie is in Nederland niet toegestaan.
Embryo-glue
Veel andere landen en buitenlandse privé-klinieken zijn minder terughoudend. Mastenbroek: “Als je in Groot-Brittannië een kliniek binnenkomt omdat je ivf wilt, krijg je letterlijk een soort menukaart voorgelegd: ‘Wilt u daar assisted hatching bij?’ ‘En embryo-glue?’ ‘Wilt u ook de time-lapse incubator gebruiken?’ Er staan per add-on gewoon prijzen achter. Patiënten, kwetsbaar als ze zijn, vinken aan wat ze hopen dat helpt. Die add-ons betalen ze zelf. Embryo-glue: 300 pond extra. Time-lapse: 700 pond extra. PGS: 3000 tot 5000 pond extra. Met als resultaat dat daar momenteel bij 75 procent van de ivf-behandelingen add-ons worden toegepast.”

Lambalk: “Maar of het nou wel of niet werkt: dit is wat gebeúrt. Grof gesteld in alle landen behalve Nederland. Vruchtbaarheidsbehandelingen zijn big business. En dat vind ik verwerpelijk. Vooral wanneer artsen add-ons slijten waarvan is aangetoond dat ze niet-effectief zijn.”
De motivatie om niet-effectieve add-ons toch aan te bieden aan wensouders is vooral commercieel, stellen Lambalk en Mastenbroek: er valt veel geld mee te verdienen. Het Nederlandse ziekenhuissysteem kent die perverse prikkel niet. Mastenbroek: “Onze situatie is heel anders dan die in het buitenland. Wij kunnen veel objectievere besluiten nemen omdat onze salarissen niet gekoppeld zijn aan het aantal en het type behandelingen dat we doen. In veel buitenlanden wordt de hoogte van het salaris, of dat van de eigenaar van de kliniek, daardoor bepaald. Dan ben je snel geneigd allerlei behandelingen te doen.”
'Kweekembryo's'
Bij Amsterdam UMC lopen diverse onderzoeken die de embryologie vooruit moeten helpen, waarbij de eigen kritische blik de norm is. Mastenbroek ziet kansen voor de verbetering van de kennis door te bestuderen wat er gebeurt tijdens de allereerste drie, vier dagen na de bevruchting van een embryo. Mastenbroek: “De embryo’s waaraan wij nu onderzoek doen, blijven over na ivf; die zijn dus minimaal een dag of vier oud. De informatie die we uit jongere embryo’s zouden kunnen halen, krijgen we dus nooit te zien."

"Als we onderzoek bij embryo’s zouden mogen doen die daarvoor speciaal tot stand worden gebracht, dan kunnen wij de voorplantingsgeneeskunde verbeteren. We zouden dan de gedragingen kunnen zien van het embryo gedurende de eerste drie dagen van de celdeling. Dat zijn nu juist de dagen dat het embryo zich tijdens de ivf-behandeling in het laboratorium bevindt.”
“Daarom pleiten wij ervoor dat we de eicellen en de zaadcellen die door mensen aan ons worden gedoneerd, maar die niet worden ingezet voor ivf, bij elkaar mogen brengen voor embryo’s die niet bedoeld zijn om er een baby uit te laten groeien, maar om er fundamenteel wetenschappelijk onderzoek aan te kunnen doen. En onderzoek naar de effectiviteit van de huidige ivf-methoden. Zogeheten ‘kweekembryo’s'. Helaas mogen we die tot nu toe niet maken van de wet. We hopen dat daar verandering in komt.”
Tekst: Mieke Zijlmans
Foto’s: Marieke de Lorijn
Dit verhaal verscheen in ons populair-wetenschappelijke tijdschrift Janus.




