"Via je ene arm nemen ze bloed af, ze halen de T-cellen eruit, en via de andere arm stroomt het terug je lichaam in", vertelt Clark. "Je T-cellen gaan voor bewerking naar de Verenigde Staten. Ik heb ruim zes weken moeten wachten tot de bewerkte cellen terugkwamen. Het moeilijke was dat ik in die periode moest stoppen met de medicijnen die de celgroei remmen. Dus ik werd zieker en zieker.”
“Het teruggeven van de CAR-T-cellen gaat heel snel, via een infuus. De dag erna kreeg ik koorts. Mijn bloeddruk daalde enorm, daarom werd ik naar de IC gebracht. Toen ik stabiliseerde, kon ik terug naar de afdeling. Daar kreeg ik een out-of-body-experience: ik zweefde boven mezelf, zag mezelf liggen. Dat komt doordat er cytokines, boodschapperstoffen tussen de afweercellen, naar je hersens gaan. De supercharged cellen gaan tekeer tegen de kanker, en dat is de bedoeling ook. Veel kankercellen gaan dood, dat levert een cytokine-storm op. Daar word je heel ziek van.”
“De arts geeft je steroïden om die cytokinenstorm te dempen, en dat moet perfect worden getimed. Als je de steroïden te vroeg geeft, dan gaat de kanker niet weg, en genees je niet. Maar geef je ze te laat, dan ga je dood. Ik heb dan ook enorme bewondering voor die dokter!”
“Inmiddels zijn we ruim tweeënhalf jaar verder. Onder andere mijn bloedwaarden zijn van slag. Ik kan nog steeds zelf geen afweereiwitten aanmaken. Daarom krijg ik maandelijks een infuus met deze eiwitten. Natuurlijk heb ik soms donkere momenten, maar ik geniet van elke dag. Deze behandeling is een ongelooflijke doorbraak in de behandeling van lymfeklierkanker.”
CAR T-celtherapie: hoe werkt het?
T-cellen zijn witte bloedcellen, afweercellen die in het bloed zitten. Wanneer ze in aanraking komen met een lichaamsvreemde stof, vermenigvuldigen ze zich. Met behulp van receptoren, een soort antennes, hechten ze zich aan de indringer en vernietigen die.
Bij onder andere lymfeklierkanker herkennen de T-cellen de kwaadaardige cellen onvoldoende als lichaamsvreemd. Om die T-cellen beter toe te rusten, waarna ze de kankercellen wél zien en onschadelijk maken, is CAR-T-celtherapie ontwikkeld. Daartoe worden de T-cellen uit het bloed van de patiënt gefilterd om ze vervolgens te versterken.
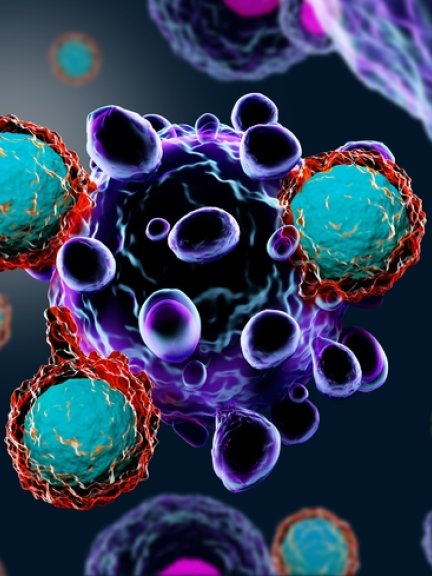
Dat versterken gaat als volgt: in het laboratorium wil je de T-cellen zo ver krijgen dat ze het eiwit CAR (Chimere Antigeen Receptor) gaan maken. CAR is een verbindend tussenstukje dat buiten op de T-cel gaat zitten en dat de structuur van de kankercellen herkent. Omdat je dit eiwit niet zomaar in een T-cel kunt stoppen, wordt een onschuldig virus gebruikt om de genetische code voor CAR in de T-cel te brengen. De T-cel leest die genetische code af en gaat het eiwit maken. Teruggebracht in het lichaam, binden deze CAR- T-cellen zich aan de kankercellen. Daarbij komen stoffen vrij waarmee ze die kunnen doden.
Eén cel kan meerdere kankercellen doden. Bewerkte T-cellen vermenigvuldigen zich, en ze hebben een geheugenfunctie die altijd aangewakkerd kan worden om kanker opnieuw te herkennen. Daarom hoef je een patiënt er maar één keer mee te behandelen.
Onderzoekers verwachten dat CAR-T-celtherapie in de toekomst geschikt zal zijn om verschillende soorten lymfeklierkanker, acute lymfatische leukemie en multipel myeloom te behandelen. Vooralsnog lijkt de therapie minder effectief voor vormen van kanker waarbij patiënten solide tumoren hebben (gezwellen die ontstaan in organen of weefsels). Er wordt echter volop onderzoek gedaan om de werking bij zulke tumoren te verbeteren.
Tekst: Mieke Zijlmans
Foto: Marieke de Lorijn